اگزالیک اسید در شکل پودری، ممکن است که این ماده در دو یا چند شکل مختلف وجود داشته باشد. پیوند هیدروژنی موجود در این اسید به توسعه ساختار زنجیره مانند در سطح بین مولکولی کمک میکند. چند شکل دیگری از این ترکیب نیز در معرض پیوند هیدروژنی قرار دارد؛ اما در این مورد پیوند هیدروژنی یک ساختار ورقه مانند را به ترکیب در سطح بین مولکولی پیوند میدهد. این محصول با توجه به ماهیت اسیدی که دارد آن را برای واکنش های استری شده ایدهآل میکند.
اگزالیک اسید چیست؟
اسید اگزالیک یک ترکیب آلی بوده که در بسیاری از سبزیجات و گیاهان نیز موجود میباشد. این ماده ساده ترین نوع از اسید دی کربوکسیلیک است. ناگفته نماند که این محصول را میتوان به طور مصنوعی در آزمایشگاه با اکسیداسیون ساکارز در حضور اسید نیتریک تهیه کرد. این ماده از اکسیداسیون کربوهیدراتها تولید میشود ضمن اینکه در این تولید به کاتالیزور پنتوکسید وانادیوم نیاز دارد. فرمول متراکم آن COOH-COOH بوده که نشان دهنده اگزالیک اسید دی بازیک در طبیعت است.
این ماده یکی از ترکیبات اگزالات کلسیم است که ترکیب رایج سنگ کلیه میباشد. سبزیجاتی از خانواده اسفناج و براسیکا مانند کلم، کلم بروکلی و کلم بروکسل سرشار از اگزالات هستند. همچنین بدن انسان نیز میتواند آن را با متابولیسم اسید گلیوکسیلیک یا اسید اسکوربیک تولید کند. از دیگر خاصیت های مهم آن داشتن طبیعت آبدوست، است. لازم به ذکر است که مصرف زیاد از این ماده برای سلامتی خطرناک میباشد.
تاریخچه تولید اگزالیک اسید
برای اولین بار در سال 1745 گیاه شناس و پزشک هلندی هرمان بورهاو، نوعی ماده را از خاکشیر جدا کرد این جداسازی مواد منجر به کشف اگزالیک اسید شد. در سال 1773، اسید اگزالیک از این ماده در خاکشیر توسط فرانسوا پیر ساواری جدا سازی گردید.
شیمیدانان سوئدی کارل ویلهلم شیل و توربرن اولوف برگمان این ماده را با واکنش قند با اسید نیتریک غلیظ تولید کردند. شیل، اسید حاصل را ساکر سیرا به معنی اسید قند یا اسید شیرین نامیده است. در سال 1784 ثابت شد که اسید قند و اسید اگزالیک به دست آمده در طبیعت یکسان هستند.
در سال 1824، فریدریش ولر، شیمیدان آلمانی، دوباره این محصول را با واکنش سیانوژن و آمونیاک در محلول آبی تولید کرد. این آزمایش را میتوان اولین سنتز یک محصول طبیعی در نظر گرفت.

تهیه اسید اگزالیک
اسید اگزالیک را میتوان در آزمایشگاه ها با اکسیداسیون کربوهیدرات های خاص مانند ساکارز توسط اسید نیتریک غلیظ، تهیه کرد. در طی فرآیند اکسیداسیون، اتم های کربن به صورت جفتی برای تولید این محصول تقسیم میشوند.
10گرم نیشکر را در یک فلاسک مخروطی ریخته سپس 50 میلیلیتر اسید نیتریک غلیظ را اضافه کنید و روی بخار اب جوش حرارت دهید؛ سپس فلاسک را برداشته و روی سطح چوبی بگذارید. پس از 15 دقیقه محلول داغ را در ظرف تبخیر ریخته و فلاسک را با 10 میلیلیتر اسید نیتریک غلیظ شسته و به ظرف تبخیر اضافه کنید.
اجازه دهید محلول اسید با حرارت دادن از طریق بخار آب جوش تبخیر شود. این کار را به حدی ادامه داده تا محلول باقیمانده به حدود 10 میلی لیتر برسد. محلول را در مخلوط آب یخ، خنک کنید تا کریستالهای آن تشکیل شود. محصول را روی قیف بوشنر پمپ جمع آوری کرده، سپس آن را بین کاغذ صافی فشار داده و در هوا خشک نمایید. این ماده حدود 3.5 گرم اسید اگزالیک خواهد بود.
در مقیاس بزرگ، اگزالات سدیم با جذب مونواکسیدکربن تحت فشار درهیدروکسید سدیم داغ تولید میشود. این ماده را به صورت جامد نیز میتوان با گرما یا با تقطیر آزئوتروپیک آبگیری کرد به طور معمول این ماده به عنوان دی هیدرات به دست میآید. اسید اگزالیک بی آب بهصورت دو شکل وجود دارد، در یکی، پیوند هیدروژنی منجر به ساختاری زنجیرهوار میشود، در حالی که الگوی پیوند هیدروژنی در شکل دیگر ساختاری ورقه مانند را دارا است.
موارد استفاده از اسید اگزالیک
این ماده در انواع صنایع کاربرد دارد از جمله؛
- استفاده در فرآیند رنگرزی به عنوان یک ماده خشک کننده مفید
- به عنوان اسید شوینده قوی در پودرهای لباس شویی
- استفاده برای از بین بردن فلسها
- استفاده به عنوان سفیدکننده در انواع مواد
- مورد استفاده در فرآیند استخراج فلزات لانتانید و به عنوان یک عامل کاهنده
- برای درخشش در مجسمه های مرمری کاربرد دارد
- قابل استفاده برای از بین بردن لکه های غذا و جوهر
- کاربرد بالا در توسعه فیلم و عکاسی
- برای حذف رسوب کلسیم در تصفیه فاضلاب
- در تولید درمان های ضد زنگ (مغازه های خودرو و برای بازسازی اشیای عتیقه)
- به عنوان افزودنی در پاک کننده های چرخ خودرو
- برای صیقل دادن سطح سنگ و مرمر
- به عنوان درمان برای از بین بردن زگیل
همچنین از تبخیر شده این ماده یا محلول 6 درصد اگزالیک اسید در شربت قند، برخی از زنبورداران به عنوان حشره کش علیه کنه انگلی استفاده میکنند. استفاده در ترمیم کننده های چوب که اسید، لایهای از سطح چوب را خشک میکند تا مواد تازه زیر آن در معرض دید قرار گیرد.
افزایش کاربرد اسید اگزالیک در صنعت داروسازی
گسترش روزافزون صنعت داروسازی در سراسر جهان، فرصتهای رشد جدیدی را در بازار اسید اگزالیک ایجاد میکند. مردم برای مقابله با خطر بیماری ها و آلرژی ها مقدار زیادی از درآمد خود را صرف خرید دارو میکنند.
این ماده به طور فزایندهای برای تولید داروهای بی شماری مانند بورنئول، ترامسیین و تتراسایکلین استفاده میشود. این محصول به یک ماده ضروری در برخی از محصولات سفید کننده دندان تبدیل شده است. از این رو، افزایش آگاهی در مورد مراقبت از دهان و تقاضا برای این محصولات پزشکی، فروش آن را افزایش میدهد. علاوه بر این، افزایش نگرانیها در مورد افزایش عفونتهای محل جراحی در سرتاسر جهان باعث شده که تقاضا برای این نوع مواد افزایش یابد.
اثرات فیزیولوژیکی اسید اگزالیک
گاهی اوقات یون های فلزی دو ظرفیتی در تشکیل رسوبات نامحلول، برعکس عمل میکنند؛ مثلاً اسید اگزالیک در بدن انسان، با یونهای فلزاتی مانند کلسیم، فلوراید، منیزیم، ترکیب شده تا کریستالهای اگزالات را رسوب دهد که لازم به ذکر است این ماده سبب تحریک روده و کلیهها میگردد. زیرا مواد مغذی حیاتی مانند کلسیم را به هم متصل میکند، مصرف طولانی مدت غذاهای حاوی اسید اگزالیک میتواند مشکل ساز باشد.
افراد سالم میتوانند با خیال راحت چنین غذاهایی را در حد اعتدال مصرف کنند، اما به افرادی که دارای اختلالات کلیوی، نقرس، آرتریت روماتوئید یا اشکال خاصی از درد مزمن فرج هستند (ولودینیا) معمولاً توصیه میشود از غذاهای حاوی اگزالات زیاد خودداری کنند و این برعکس مکملهای کلسیم است که همراه با غذاهای حاوی اگزالیک اسید بالا مصرف میشود زیرا میتوانند باعث رسوب اگزالات کلسیم در روده گردیده و سطح اگزالات جذب شده توسط بدن را به شدت کاهش دهند در برخی موارد تا 97% کلسیم رسوب اگزالات (که بیشتر به عنوان سنگ کلیه شناخته میشود) لولههای کلیه را مسدود میکند.
اسید اگزالیک همچنین میتواند توسط متابولیسم اتیلن گلیکول (ضد یخ) اسید گلیوکسیلیک یا اسید اسکوربیک تولید شود. این ماده میتواند تحت شرایط خاصی از غلظت و pH، به صورت بلورهای اگزالات کلسیم در کلیهها رسوب کند و تقریباً 80 درصد سنگهای کلیه را تشکیل دهد.
برخی از گونههای آسپرژیلوس این ماده را تولید میکنند که با خون یا کلسیم بافت واکنش داده و اگزالات کلسیم را رسوب دهد. شواهد اولیهای وجود دارد که نشان میدهد تجویز پروبیوتیک ها میتواند بر میزان دفع این ماده تأثیر بگذارد.
چگونه میتوان اگزالات را از بدن خارج کرد؟
این کار با افزایش مقدار کلسیم در رژیم غذایی امکانپذیر است. رژیم غذایی سرشار از کلسیم به کاهش میزان اگزالات جذب شده توسط بدن انسان کمک میکند، و در نتیجه احتمال تشکیل سنگ کلیه را کمتر
برخی از خطرات اسید اگزالیک برای سلامتی چیست؟
اسید اگزالیک بسیار سمی بوده و از این رو بسیار مضر و خطرناک است. در صورت استنشاق، میتواند به غشاهای مخاطی و همچنین دستگاه تنفسی و کلیه ها آسیب جدی وارد نماید. علاوه بر این، علائمی مانند سرفه، خس خس سینه، لارنژیت و تنگی نفس نیز نشان دهنده مسمومیت ناشی از این ماده میباشد. تماس آن با پوست یا چشم ممکن است باعث تحریک شدید، سوختگی و آسیب بافتی گردد همچنین در هنگام بلعیدن سمی بوده و از این رو ممکن است منجر به نارسایی کلیه شود. این سمیت زمانی ایجاد میشود که با کلسیم موجود در بافت های بدن انسان واکنش یابد و اگزالات کلسیم را تشکیل دهد و در نتیجه نسبت کلسیم پتاسیم را به هم زند.
اسید اگزالیک در طبیعت
اگزالات ها به وفور در بسیاری از گیاهان وجود دارد، مانند علف ترش و خاکشیر ریشه و یا برگ های ریواس و گندم سیاه که همگی دارای اسید اگزالیک فراوان میباشند.
میوههای (کارامبولا)، فلفل سیاه، جعفری، دانه خشخاش،ساقه ریواس، تاج خروس، اسفناج، شاتوت، چغندر، کاکائو، شکلات، بیشتر مغزها، انواع توتها و لوبیاها دارای این ماده هستند.
آیا اسید اگزالیک اسیدی قوی است؟
این اسید به عنوان یک اسید آلی، اسیدی ضعیف است و به عنوان اسید نرم شناخته شده، در حالی که از اسید استیک، اسید سولفوریک، اسید نیتروز، اسید بنزوئیک و … قویتر و بهتر عمل میکند.
بازار جهانی اسید اگزالیک
این اسید یکی از سمی ترین مواد شیمیایی در جهان بوده با این حال استفاده از آن در بسیاری از صنایع، با افزایش روبه روست. این ماده باعث نارسایی کلیه شده که در اثر رسوب اگزالات کلسیم جامد ایجاد میشود. تمایل اسید اگزالیک برای متصل شدن به مواد معدنی موجود در روده و جلوگیری از جذب آن سبب افزایش غلظت اگزالات شده که این اتفاق منجر به تشکیل سنگ کلیه میشود.
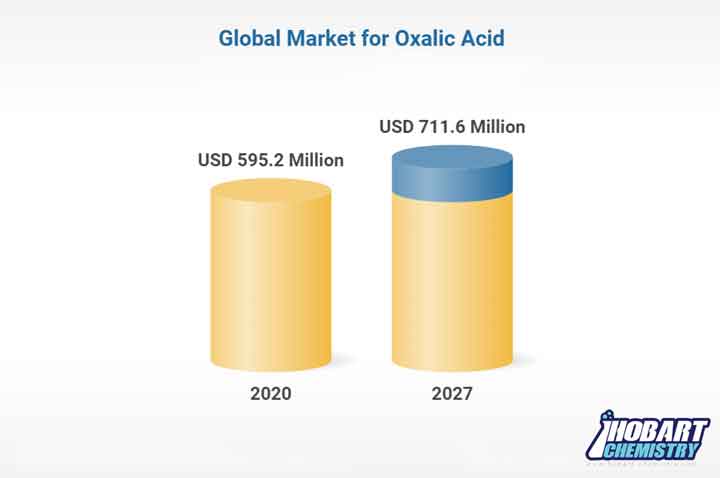
باتوجهبه شرایط و مقدار استفاده این محصول در صنایع، بر آورد شده که بازار جهانی آن تا سال 2027 به ارزش 711.6 میلیون دلار برسد و با رشدی 2.6% CAGR داشته باشد. در دوره تجزیه و تحلیل 2020-2027 دی هیدرات، یکی از بخش های مورد تجزیه و تحلیل در گزارش است که پیش بینی میشود این ماده به سبب تولید اگزالیک اسید 3% CAGR را ثبت کند و تا پایان دوره تجزیه و تحلیل به 341.8 میلیون دلار برسد.
خرید اگزالیک اسید
مجموعه بزرگ هوبارت شیمی جزو برترین های بازار فروش مواد شیمیایی بوده که این ویژگی، فروش بالای انواع مواد را از این مجموعه سبب شده است. تمامی مواد شیمیایی تهیه و ارائه شده توسط این شرکت تحت نظر کارشناسان و شیمیدانان متخصص به انجام میرسد. محبوبیت بالای این مجموعه در بازار، سبب فروش بالای محصولاتش گشته، همچنین جای هیچ گونه نگرانی در هنگام تهیه مواد از این مجموعه وجود ندارد زیرا اصل بودن و خالص بودن آن توسط مصرف کنندگان به اثبات رسیده است. شما عزیزان گرامی در صورت نیاز به خرید و مشاوره به صورت شبانه روزی میتوانید با مشاوران ما تماس حاصل نمایید و در خرید و تهیه مواد مورد نیاز راهنمایی بخواهید دستاندرکاران این مجموعه با کمال میل در خدمت شما هستند.










نقد و بررسیها
هیچ دیدگاهی برای این محصول نوشته نشده است.